|

Ионы водорода в природной воде обусловлены диссоциацией угольной кислоты. Большинство природных вод имеют pH в пределах 6,5 - 8,5. Для поверхностных вод в связи с меньшим содержанием в них углекислоты pH обычно выше, чем для подземных.
Соединения азота в природной воде представлены ионами аммония, нитритными, нитратными ионами за счет разложения органических веществ животного и растительного происхождения. Ионы аммония, кроме того, попадают в водоемы со сточными промышленными водами.
Соединения железа очень часто встречаются в природных водах, причем переход железа в раствор может происходить под действием кислорода или кислот ( угольной, органических(. Так например, при окислении весьма распространенного в породах пирита получается сернокислое железо:
FeS2 + 4O2 ® Fe2+ + 2SO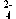
а при действии угольной кислоты - карбонат железа:
FeS2 + 2H2CO3 ® Fe2+ + 2HCO3 + H2S + S.
Соединения кремния в природных водах могут быть в виде кремниевой кислоты. При pH < 8 кремниевая кислота находится практически в недиссоциированном виде; при pH >8 кремниевая кислота присутствует совместно с HSiO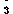 , а при pH >II - только HSiO , а при pH >II - только HSiO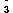 . Часть кремния находится в коллоидном состоянии, с частицами состава HSiO2·H2O , а также в виде поликремнеивой кислоты: X·SiO2··H2O. В природных водах присутствуют также Al3+ ,Mn2+ и другие катионы. . Часть кремния находится в коллоидном состоянии, с частицами состава HSiO2·H2O , а также в виде поликремнеивой кислоты: X·SiO2··H2O. В природных водах присутствуют также Al3+ ,Mn2+ и другие катионы.
Помимо веществ ионного тапа природные воды содержат также газы и органические и грубодисперсные взвеси. Наиболее распространенными в природных водах газами являются кислород и углекислый газ. Источником кислорода является атмосфера, углекислоты - биохимические процессы, происходящие в глубинных слоях земной коры, углекислота из атмосферы.
Из органических веществ, попадающих извне, следует отметить гуминовые вещества, вымываемые водой из гумусовых почв (торфяников, сапропелитов и др.). Большая часть из них находится в коллоидном состоянии. В самих водоемах органические вещества непрерывно поступают в воду в результате отмирания различных водных организмов. При этом часть из них остается взвешенной в воде, а другая опускается на дно, где происходит их распад.
Грубодисперсные примеси, обуславливающие мутность природных вод, представляют собой вещества минерального и органического происхождения, смываемые с верхнего покрова земли дождями или талыми водами во время весенних паводков.
Подземные воды.
Советский ученый Лебедев на основе многочисленных экспериментов разработал классификацию видов воды в почвах и грунтах. Представления А.Ф.Лебедева, получившие дальнейшее развитие в более поздних исследованиях, позволили выделить следующие виды воды в горных породах: в форме пара, связанную, свободную, в твердом состоянии.
Паро-образованная вода занимает в породе поры, не заполненные жидкой водой, и перемещается за счет различной величины упругости пара или потоком воздуха. Конденсируясь на частицах породы, водяные пары переходят в другие виды влаги.
Различают несколько видов связанной воды. Сорбированная вода удерживается частицами породы под влиянием сил, возникающих при взаимодействии молекул воды с поверхностью этих частиц и с обменными катионами. Сорбированную воду разделяют на прочносвязанную и рыхлосвязанную. Если влажную глину подвергать давлению, то даже под давлением в несколько тысяч атмосфер часть воды невозможно удалить из глины. Это прочносвязанная вода. Полное удаление такой воды достигается лишь при температуре 150 - 300оС. Чем меньше минеральные частицы, слагающие породу, и, следовательно, выше их поверхностная энергия, тем большее количество прочносвязанной воды в этой породе. Рыхлосвязанная, или пленочная, вода образует плёнку вокруг минеральных частиц. Она удерживается слабее и довольно легко удаляется из породы под давлением. Особенно важную роль играет сорбированная вода в глинистых породах. Она влияет на прочностные свойства глин и фильтрационную способность.
Как уже указывалось, связанная вода участвует в строении кристаллических решёток некоторых минералов. Кристаллизационная вода входит в состав кристаллической решётки. Гипс, например содержит две молекулы воды CaSO4·2H2O. При нагревании гипс теряет воду и превращается в ангидрит (CaSO4).
Перейти на страницу: 1 2 3 4 5 6 |